Ngày 20/11, Phó Cục trưởng Cục Quản lý dược - Bộ Y tế, Đỗ Văn Đông vừa ký quyết định số 701/QĐ-XPHC xử phạt vi phạm hành chính đối với công ty Windlas Biotech Pvt.Ltd (Ấn Độ) - đại diện là Công ty cổ phần dược phẩm Khánh Hòa.


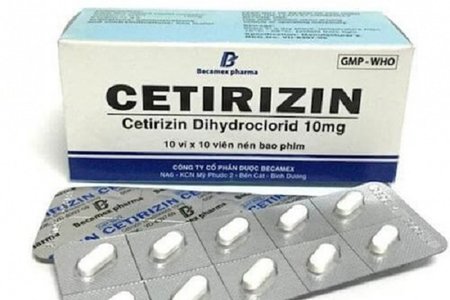
Công ty nói trên có hành vi vi phạm là: sản xuất thuốc Cetirizine 10mg không đạt tiêu chuẩn chất lượng mức độ 2 theo quy định của pháp luật.
Ngoài mức xử phạt vi phạm hành chính là 70 triệu đồng, Cục Quản lý dược yêu cầu Công ty cổ phần dược phẩm Khánh Hòa và các đơn vị liên quan phải thực hiện thu hồi triệt để, tiêu hủy toàn bộ lô thuốc kém chất lượng nêu trên.
Cùng ngày, tại quyết định số 700/QĐ-XPHC, Cục Quản lý dược xử phạt vi phạm hành chính đối với công ty Pharmix Corporation (đại diện cho nhà sản xuất - Công ty Crown Pharm.Co., Ltd) vì hành vi sản xuất thuốc Sebemin (SĐK VN-14320-11, số lô SDM1711) không đạt tiêu chuẩn chất lượng mức độ 2 theo quy định của pháp luật.
Mức xử phạt là 70 triệu đồng. Cục Quản lý dược yêu cầu Công ty Pharmix Corporation phối hợp với các đơn vị liên quan thực hiện thu hồi và huỷ toàn bộ lô thuôc kém chất lượng nêu trên theo quy định hiện hành.
Tại Quyết định số 699/QĐ-XPHC, Cục Quản lý dược xử phạt vi phạm hành chính đối với Công ty Flamingo Pharmaceuticals Ltd (Văn phòng đại diện tại quận Hà Đông, Hà Nội) vì thực hiện hành vi sản xuất thuốc thuốc Clavophynamox 1000 (SĐK VN-20275-17, số lô K026) không đạt tiêu chuẩn chất lượng mức độ 3 theo quy định của pháp luật.
Mức xử phạt với công ty này là 40 triệu đồng. Cục Quản lý dược cũng yêu cầu công ty Flamingo Pharmaceuticals Ltd phối hợp với các đơn vị liên quan thực hiện thu hồi triệt để và hủy toàn bộ lô thuốc kém chất lượng nêu trên theo quy định hiện hành.